1. デング熱流行の背景:深刻化する世界的な公衆衛生上の課題
デング熱は、デングウイルス(DENV)によって引き起こされる急性蚊媒介性ウイルス疾患であり、世界で最も急速に拡大しているアルボウイルス疾患として出現し、公衆衛生の安全保障に大きな脅威をもたらしています。過去20年間で、デング熱の世界的な発生率は劇的に増加しており、報告された症例数は2021年以降毎年倍増しています[1]。2023年12月、世界保健機関(WHO)は、国際的な協調対応を強化するために、世界的なデング熱緊急事態を宣言しました。WHOの疫学的推定によると、世界中で約39億人がデング熱感染のリスクにさらされており、年間推定3億9000万人が感染し、そのうち9600万人が臨床的に明らかな症例として現れています[1,2]。
2. 疫学的ハイライト
デング熱の疫学的特徴は、ウイルス学的要因、媒介生物の生態、宿主の免疫応答、および社会環境条件の相互作用によって形成される。これらの特徴を包括的に理解することは、効果的な予防・制御戦略および正確な診断手法の開発に不可欠である。
2.1 感染経路と都市部における感染パターン
デングウイルスは主にネッタイシマカとヒトスジシマカ蚊。これらの媒介種の中で、ネッタイシマカ(Aedes aegypti)は最も重要な感染媒介種として認識されており、高い「ヒトへの適応性」と熱帯および亜熱帯の都市環境における広範な分布を特徴としています。アルボウイルス病原体の他の蚊媒介種とは異なり、ネッタイシマカは以下の重要な疫学的特徴を示します。
・人工的な環境(例:貯水容器、廃棄タイヤ)での繁殖を好む
栄養源としてヒトの血液に対する強い親和性を持つ
日中の摂食行動
これらの特徴はデング熱を典型的な「都市型感染症」人口密度の高い地域では、伝播効率が著しく上昇します。WHO関連の研究では、高密度の都市部では、蚊と人間の接触頻度の増加により、デングウイルスの基本再生産数(R₀)が大幅に上昇し、それによって流行の拡大が加速することが実証されています[2]。
2.2 世界的な感染拡大の傾向と要因
世界保健機関(WHO)の報告によると、過去20年間でデング熱の症例数は世界的に急激に増加している[1,3]。この増加傾向は主に以下の相互に関連する要因によって引き起こされている。
(1)気候変動:地球温暖化は、蚊媒介生物の生息に適した地理的範囲を拡大するだけでなく、蚊の宿主内でのデングウイルスの潜伏期間を短縮し、それによって感染効率を高めます。気候変動による蚊の密度の変化は、デング熱の発生の時空間的変動を予測する信頼できる指標としてWHOによって検証されています。
(2)都市化:急速かつ無計画な都市拡大により、蚊媒介生物の繁殖地が豊富になり、人口密度の増加によりデングウイルスの伝播連鎖の継続性が強化された。
(3)世界的な人口移動:国際的な旅行や貿易により、デングウイルスの国境を越えた急速な伝播が促進され、輸入症例から持続的な地域内感染への移行が促進されています。WHOの監視データによると、2010年から2021年の間に、米国では旅行に関連したデング熱症例が7,528件報告され、そのうち3,135件が入院を必要とし、19件が死亡に至りました。
(4)ベクター分布の拡大:世界的に、ネッタイシマカとヒトスジシマカの地理的範囲は拡大し続けており、ヨーロッパの一部地域ではネッタイシマカがますます定着しつつあります。その結果、デング熱は従来地域的な流行病であったものが、世界的な公衆衛生上の脅威へと変化しました。
2.3 複数血清型の同時流行と再感染のメカニズム
デングウイルスは、抗原的に異なる4つの血清型(DENV-1~DENV-4)から構成されています。1つの血清型に感染すると、その特定の血清型に対する長期的な防御免疫が得られますが、他の3つの血清型に対する交差防御は一時的かつ部分的なものにとどまります。一般の人々はデングウイルスに普遍的に感染しやすく、感染者のうち臨床症状を発症するのはごく一部です[2]。
風土病地域では、複数のデングウイルス血清型が同時に流行することが多く、その結果、個人が生涯にわたって複数回のデング熱感染を経験する可能性があります。WHOの疫学研究では、複数の血清型の同時流行が周期的なデング熱の流行の主な要因であることが特定されています[1]。
2.4 二次感染と抗体依存性増強
デング熱の疫学における重要かつ特異な現象は抗体依存性増強(ADE)異種DENV血清型による二次感染の際、一次感染時に産生された非中和抗体がウイルスの単球およびマクロファージへの侵入を促進し、それによってウイルス複製を増強する。このメカニズムは、デング出血熱やデングショック症候群を含む重症デング熱の主要な病原性因子としてWHOによって広く認識されている[1]。
WHOの疫学データは、二次感染したデング熱患者は一次感染した患者に比べて重症化するリスクが著しく高いことを一貫して示しており、これは疾病監視と臨床管理において非常に重要な特徴である。二次感染では重症化するリスクが高まるが、どのデングウイルス血清型でも重症デング熱に進行する可能性があることに注意する必要がある[1]。
2.5 非特異的な臨床症状と誤診のリスク
デング熱の臨床症状は、特に病気の初期段階では非特異的であり、他の蚊媒介性ウイルス感染症(チクングニアウイルスやジカウイルスなど)や特定の呼吸器感染症の症状と重複することが多い。WHOの推定では、DENV感染の40~80%は無症状である[3]。
典型的な臨床症状は以下のとおりです。
-急性発熱(2~7日間持続し、二相性の場合もある)
・激しい頭痛と眼窩後部痛(目の奥の痛み)
・筋肉痛や関節痛(一般的に「骨折熱」と呼ばれる)
斑状または斑丘疹状の発疹
軽度の出血症状(例:皮下出血、鼻血、歯肉出血)
症候性デング熱は、通常、発熱期、重篤期、回復期の3つの段階に分けられます。症候性患者のうち、重症デング熱に進行するのは約5%未満です。特異的な臨床的特徴がないため、臨床症状のみに基づく診断は困難であり、誤診や診断漏れのリスクが高まります。WHOは、臨床診断だけでは正確性を確保するには不十分であり、検査室での確認が不可欠であることを明確に強調しています[1]。
WHOの「デングウイルス検査に関する暫定ガイダンス(2025年4月)」からの3つの重要ポイント
2025年4月、世界保健機関(WHO)は、デングウイルス(DENV)の検査に関する最新の暫定ガイダンスを発表し、世界的なデング熱診断のための権威ある技術指針を提供しました。このガイダンスは、現在進行中の世界的なデング熱緊急事態を踏まえ、デング熱の検査に関する最新のエビデンスを統合し、資源レベルの異なる環境に合わせた実践的な推奨事項を示しています。

3.1 テスト戦略の基本原則
このガイドラインでは、デング熱の診断には病期に基づいたマルチマーカー複合検査戦略を採用する必要があると強調している[1]。普遍的な診断アルゴリズムが存在しないため、検査戦略は地域の疫学的状況に合わせて調整する必要があり、以下の重要な要素を考慮に入れる必要がある[1]。
感染段階:症状発現後の日数によって、最も適切な検査方法が決定されます。
-検体タイプ:デングウイルス検出における全血、血漿、または血清の適合性
地域疫学:地域で流行しているデングウイルス血清型と他のアルボウイルスの同時流行
-重複感染のリスク:アルボウイルスが重複して流行している地域では、異なる病原体を区別するためにマルチプレックス検査を検討すべきである。
3.2 段階別テスト戦略
WHOのガイダンスによると、デング熱の検査は、病気の段階に基づいて明確な時間枠に従って行うべきである[1,2]。
(1)急性期検査(発症後7日以内)
-核酸検査(分子検査):逆転写ポリメラーゼ連鎖反応(RT-PCR)およびその他の分子生物学的手法により、DENV RNAを高感度で検出します。
-抗原検査:NS1抗原の検出。発症後1~3日以内に検出可能となる。
急性期にはウイルス血症レベルが比較的高く、核酸検査と抗原検査は最適な感度を発揮する。
(2)回復期検査(発症後4日以上経過)
-血清学的検査:IgM抗体は通常、発症後4日目頃から検出可能になります。
ほとんどの場合、IgM抗体は14~20日間持続しますが、場合によっては90日間持続することもあります。
-IgG検査は、過去のフラビウイルス感染やワクチン接種による交差反応性抗体が存在する可能性があるため、急性デング熱の診断には限定的な価値しかない。
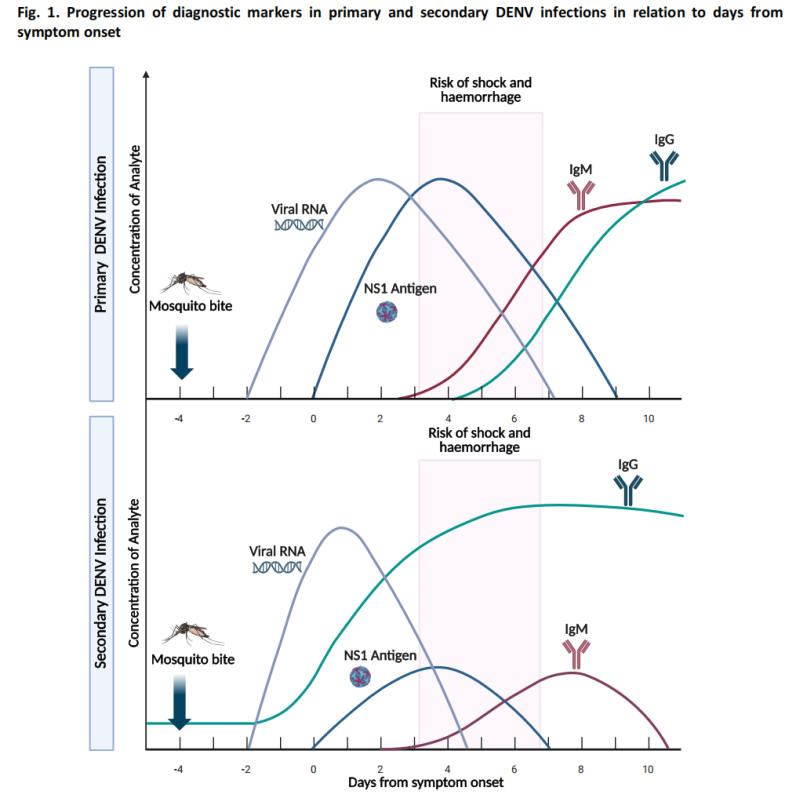
(3)疑い症例診断アルゴリズム
このガイドラインには、デング熱が疑われる症例に対する診断アルゴリズムが含まれており、症状発現後の日数に基づいて適切な検査方法を推奨している。初期段階ではNS1抗原検査と核酸検査が主なアプローチであり、後期段階では血清学的検査が主な方法である。
3.3 試験方法の性能評価と選定
世界保健機関(WHO)によると、様々なデング熱検査の性能と適用シナリオに関する体系的な評価は以下のとおりである。
| 試験方法 | ターゲット | 時間枠 | 主な適用シナリオ | 考慮事項 |
| 核酸検査 | ウイルスRNA | 発症後1~7日 | 早期確認、血清型同定 | ゴールドスタンダード法。特殊な実験機器と高度な技術が必要。 |
| NS1抗原検査 | 非構造タンパク質 | 発症後1~3日 | 早期迅速スクリーニング | 資源が限られた環境に適した迅速診断検査(RDT)形式で利用可能 |
| IgM抗体検査 | 特異的IgM抗体 | 発症後4日以上経過 | 最近の感染症の診断 | 単一の血清サンプルは、最近の感染の可能性を示唆するだけであり、確定診断には血清転換が必要です。 |
| IgG抗体検査 | 特異的IgG抗体 | 回復期/過去の感染 | 疫学的調査、免疫状態の評価 | 単一の血清サンプルは急性デング熱の診断には適していません |
| 複合検査(NS1+IgM/IgG) | 抗原+抗体 | 病気の全経過 | デング熱感染の総合診断 | 現在、デング熱診断において最も優れた性能を発揮するRDTフォーマット |
| NGS | ウイルスRNA | 発症後1~7日 | ウイルスゲノム監視 | 特殊なシーケンス装置とバイオインフォマティクス解析機能が必要 |
シナリオ別デング熱検出用マクロ・ミクロ検査製品のおすすめ4選
デング熱の予防と対策を支援するため、マクロ&マイクロテスト社は、迅速スクリーニング、分子生物学的確認、ゲノムサーベイランスを網羅した統合診断ポートフォリオを提供し、アウトブレイク管理のさまざまな段階におけるニーズに対応します。
4.1 シナリオ1:迅速なスクリーニングと標的型監視
発熱外来、一次医療施設、集団感染発生時の地域スクリーニング、港湾・国境検疫に適用可能。
-デングウイルスNS1抗原迅速検査:発症後1~3日の初期感染を検出し、15分で結果が出て迅速なトリアージを可能にします。
-デングウイルスIgM/IgG抗体検査:一次感染と二次感染を区別し、重症化リスクを評価します。
-デングウイルスNS1抗原+IgM/IgG複合迅速検査:抗原と抗体を同時に検出して、完全な診断を行います。
-チクングニアウイルスIgM/IgG抗体検査:デング熱との鑑別診断を可能にし、病原体を正確に特定します。
4.2 シナリオ2:精密診断と緊急対応
-デングウイルスI/II/III/IV核酸検出キット:アウトブレイク追跡のために4つの血清型を検出および識別します(検出限界500コピー/mL)。
-凍結乾燥デングウイルスPCRキット:室温で輸送可能で、資源が限られた地域や突発的な流行に適しています。
-デング熱/ジカ熱/チクングニア熱マルチプレックスリアルタイムPCRキット:3種類のアルボウイルスを同時に検出することで、複雑なアウトブレイクにおける効率的な鑑別診断を可能にします。

上記の試薬はすべてAIO 800全自動サンプル・トゥ・アンサーシステムに対応しており、手作業や交差汚染を減らし、効率とバイオセーフティを向上させます。
4.3 シナリオ3:ゲノム監視とウイルス系統解析
国立基準検査機関、公衆衛生研究機関に適用可能であり、WHOのNGSの位置づけに沿ったものである。
Macro & Micro-Test社のゲノムサーベイランスソリューションは、ウイルスの追跡、感染経路の解明、変異株のモニタリング、ワクチン戦略の調整のための全ゲノムシーケンス解析をサポートします。手動/自動ワークフローに対応し、スループットと再現性を向上させることで、検査機関がルーチン検査から高度なサーベイランスへと移行することを可能にし、WHOが重視するウイルス進化モニタリングの強化に貢献します。

4.4 統合ソリューションの価値
Macro & Micro-Testは、アルボウイルス検出のための包括的な診断ソリューションを提供し、アウトブレイク管理の各段階をサポートします。最前線の医療現場向けの迅速スクリーニングツール、精密診断のための分子生物学的確認、疫学的サーベイランスのための全ゲノム解析機能など、幅広いソリューションを提供しています。高性能アッセイ、柔軟なワークフロー、自動化対応プラットフォームを備えたこれらのソリューションは、世界中の検査機関や公衆衛生システムが、新たなアルボウイルス感染症の脅威に対する備えと対応を強化できるよう支援します。
参考文献
[1] 世界保健機関。デングウイルス検査:暫定ガイダンス、2025年4月。ジュネーブ:世界保健機関;2025年。
[2] WHOグローバルアルボウイルスイニシアチブ技術諮問グループ。アルボウイルス疾患の脅威に対する世界的な備えと対応の強化:行動への呼びかけ。ランセット感染症。2026;26(1):15-17。
[3] ランセット・マイクロブ。デング熱診断のジレンマを克服する。ランセット・マイクロブ。2025;6(7):101190。
投稿日時:2026年3月20日
