I. 概要ESMO2025年ガイドライン
2025年8月、ESMOは「早期および局所進行非小細胞肺癌:診断、治療、経過観察に関するESMO臨床診療ガイドライン」を正式に発表し、腫瘍学分野のトップジャーナルであるAnnals of Oncology誌に掲載しました。これは2017年版以来初の包括的な改訂版であり、世界中の腫瘍医にとって非常に権威ある参考資料となります。

肺がんは、世界中のあらゆる悪性腫瘍の中で最も発生率と死亡率が高い。毎年220万人以上が新たに肺がんと診断され、180万人以上が死亡しており、男女ともにがん関連死の主要因となっている。非小細胞肺がん(NSCLC)は、肺がん患者全体の約80~85%を占める。このような深刻な状況の中、2025年版ガイドラインの発表は、臨床現場に新たな科学的推進力をもたらし、特にバイオマーカー検査戦略のアップデートは極めて重要である。
II.主要ガイドライン改訂内容の解釈
2.1 バイオマーカー検査:「任意」から「必須」へ
2025年版ガイドラインは、バイオマーカー検査に関して画期的な戦略的調整を行っている。このガイドラインは、ステージIB~IIIの非小細胞肺がん患者における治療決定において、バイオマーカー検査が不可欠であると明記している。
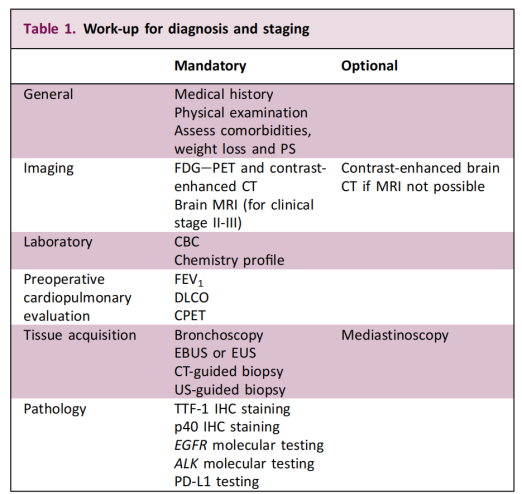
この勧告は、これまで進行期疾患の患者を対象としていた分子検査を、早期の切除可能な症例にも拡大するものです。その主な目的は、ドライバー遺伝子変異を特定し、個別化された精密医療のための科学的根拠を提供することです。また、生検の実施可能性と診断方法は、患者と腫瘍の特徴に基づいて、多職種チームによって決定されるべきであることも強調しています。
具体的な検査戦略に関して、ガイドラインでは、手術の意思決定前に遺伝子検査を実施すること、そして少なくともEGFRとALKの検査を実施することを明確に推奨しています。この「事前検査」という概念は、早期非小細胞肺癌の正確な層別化と個別化治療において、臨床的に非常に重要な意味を持ちます。検査結果の迅速性と正確さが、その後の補助療法の選択を直接左右するからです。
2.2 ドライバー遺伝子陽性早期非小細胞肺癌における治療上のブレークスルー
2025年のガイドラインは、複数の主要な臨床研究からのエビデンスを統合し、ドライバー遺伝子陽性の早期非小細胞肺がん患者に対する明確な精密治療経路を確立するものである。
EGFR変異陽性患者:画期的なADAURA試験に基づき、術後補助療法として3年間オシメルチニブを投与することが、EGFRエクソン19欠失またはエクソン21 L858R変異を有する患者に対する世界的な標準治療となっています。ADAURA試験は、完全切除されたステージIB~IIIAのEGFR変異を有する非小細胞肺癌患者における補助療法としてのオシメルチニブの有効性と安全性を評価する国際多施設共同無作為化比較第III相試験です。この試験では、オシメルチニブがプラセボと比較して無病生存期間と全生存期間の両方を有意に改善することが示され、オシメルチニブがこの集団に対する新たな標準治療として確立されました。しかし、ADAURA試験の探索的解析では、早期治療中止の約36%が有害事象によるものであり、さらに31%が患者の判断によるものであることが示されました。この結果は、持続的な利益を得られる患者に標的療法が確実に投与されるように、治療前に正確なベースライン検査を行う必要性を強調しています。
ALK陽性患者:ALINA試験に基づき、術後2年間の補助療法としてのアレクチニブ投与が標準治療となっています。第III相無作為化非盲検ALINA試験の主要解析では、アレクチニブはステージII-IIIAの患者集団において、ハザード比0.24で著明な無病生存期間延長効果を示しました。ESMO 2025学会で発表されたALINA試験の最新データでは、3年以上の追跡調査後も、ステージII-IIIAの患者集団におけるアレクチニブの無病生存期間延長効果は「持続的かつ臨床的に意義のある」ものであり、ハザード比は0.36でした。最新の報告では、4年全生存率は98.4%、4年無病生存率は75.5%に達し、中枢神経系無病生存率も改善し、新たな安全性シグナルは認められませんでした。これらの確固たるデータは、ALK陽性非小細胞肺癌切除後の補助療法としてのアレクチニブの標準治療としての地位をさらに確立し、このような患者を特定するための正確な検査の重要性を強調しています。
試験方法の選択:2025年のESMOガイドラインでは、マルチプレックスRT-PCRパネルアッセイALK融合遺伝子検出のための推奨技術手法の一つとして、RNAベースのNGS、IHC、FISHと並んで挙げられています。これは、ガイドラインの中核的な要件が、特定の検査プラットフォームを義務付けるのではなく、臨床上の意思決定を支援するための検査を実施することにあることを示しています。EGFRおよびALK検出に特化したRT-PCR製品にとって、この柔軟な検査戦略は、臨床現場での使用をガイドラインに基づいて強力に正当化するものです。
III. 精密試験技術ソリューション
2025年のガイドラインでは、検査を術前意思決定段階にまで進めており、検査の精度、感度、およびアクセス性に関する基準が引き上げられています。以下に説明する2つのRT-PCRベースの検出製品は、技術的な観点から、このガイドラインの要件に完全に合致しています。
3.1 EGFR変異検出キット – 強化型ARMSテクノロジープラットフォーム
コアテクノロジー強化されたARMS技術により、野生型配列が多いバックグラウンドに対して、低存在量の変異配列を特異的に増幅することが可能になります。
3つの技術的安全対策:
-ARMSの強化 → 突然変異の認識精度が向上
-酵素濃縮→野生型バックグラウンドを消化し、変異型配列を濃縮する
温度遮断 → 非特異的増幅を抑制する
パフォーマンス: 感度変異アレル頻度1%
汚染管理: 内蔵内部制御 + UNG酵素による汚染防止
処理時間: 密閉管式運転、約120分
サンプル適合性:組織/液体生検サンプル → 「事前テスト」要件に対応
カバレッジ:45個の変異EGFRエクソン18~21において、ガイドラインで強調表示されている領域(エクソン19の欠失およびエクソン21のL858R)と正確に一致する。
臨床使用EGFR-TKI療法を直接的にガイドする
3.2 MMT EML4-ALK融合遺伝子検出キット – RNAベースの融合遺伝子検出ソリューション

-テクノロジープラットフォームRNAベースのRT-PCRは、融合遺伝子検出においてDNAベースの方法よりも本質的に優位性がある。
-RNAベースの利点: 発現した融合転写産物を直接検出することで、偽陰性を効果的に回避します。
-研究による証拠低頻度のALK融合遺伝子の場合、RT-PCRはDNAベースの検査よりも有意に信頼性が高い。
-感度: 融合を検出します反応ごとに20コピー
-バリアントのカバー範囲: カバーEML4-ALK融合遺伝子の一般的な変異体12種類(変異体1は約33%、変異体3a/3bを合わせた割合は約29%)
-運転および汚染管理密閉チューブ、約120分;内蔵プロセス制御+UNG酵素により偽陽性結果を防止
-機器の互換性: 様々な主流のリアルタイムPCR装置に対応
-ガイドラインの整合性ESMOガイドラインと非常に整合性が高い
IV.検査法とガイドライン推奨事項との整合性
これら2つの検出製品は、以下の主要な点において、ESMO 2025早期および局所進行非小細胞肺癌ガイドラインと非常に高い整合性を示しています。
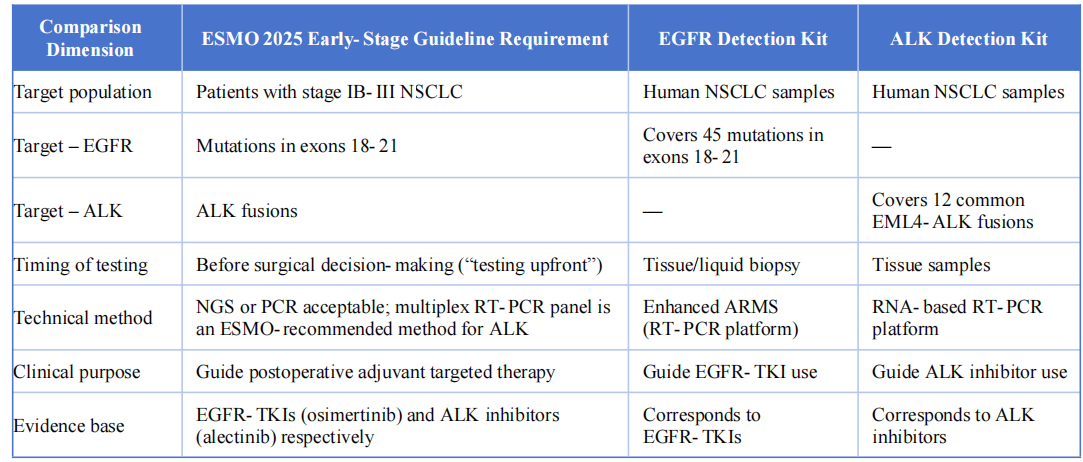
V. 結論
ESMO 2025早期NSCLCガイドラインは、精密診断と治療の新時代を切り開き、「事前の検査、精密な標的設定、そして治療の最適化。「EGFR変異検出キットとMMT EML4-ALK融合遺伝子検出キットは、それぞれ異なる技術的手法によって、標的、タイミング、精度に関するガイドラインの要件を満たしています。」
EGFRキットは、強化されたARMS技術を用いて、限られたサンプル中の標的変異を高感度で検出します。組織生検と液体生検の両方に対応し、「事前検査」を可能にします。
ALKキットはRNAベースのRT-PCRに基づいており、融合遺伝子の検出においてDNA法よりも優位性があり、ALK検査におけるマルチプレックスRT-PCRパネルの使用に関するESMOの推奨に合致している。
これら2つの製品を組み合わせることで、ESMO 2025ガイドラインに準拠した精密検査ソリューションが実現し、早期非小細胞肺がんに対する個別化補助療法を支援します。
参考文献:
- Zer A、Ahn MJ、Barlesi Fら。早期および局所進行非小細胞肺癌:診断、治療、経過観察に関するESMO臨床診療ガイドライン。Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
投稿日時:2026年5月6日

